| Jewiki unterstützen. Jewiki, die größte Online-Enzyklopädie zum Judentum.
Helfen Sie Jewiki mit einer kleinen oder auch größeren Spende. Einmalig oder regelmäßig, damit die Zukunft von Jewiki gesichert bleibt ... Vielen Dank für Ihr Engagement! (→ Spendenkonten) |
How to read Jewiki in your desired language · Comment lire Jewiki dans votre langue préférée · Cómo leer Jewiki en su idioma preferido · בשפה הרצויה Jewiki כיצד לקרוא · Как читать Jewiki на предпочитаемом вами языке · كيف تقرأ Jewiki باللغة التي تريدها · Como ler o Jewiki na sua língua preferida |
Oligomycin A
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
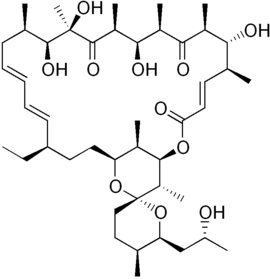
| |||||||
| Allgemeines | |||||||
| Name | Oligomycin A | ||||||
| Andere Namen |
| ||||||
| Summenformel | C45H74O11 | ||||||
| CAS-Nummer | 579-13-5 | ||||||
| PubChem | 52947716 | ||||||
| Kurzbeschreibung |
weißes Pulver[1] | ||||||
| Arzneistoffangaben | |||||||
| Wirkstoffklasse | |||||||
| Eigenschaften | |||||||
| Molare Masse | 791,06 g·mol−1 | ||||||
| Schmelzpunkt |
140–141 °C[2] | ||||||
| Löslichkeit | |||||||
| Sicherheitshinweise | |||||||
| |||||||
| Toxikologische Daten | |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Oligomycin A ist ein von Streptomyces erzeugtes Antibiotikum aus der Gruppe der Makrolide, die für andere Organismen giftig sein können. Oligomycin A ist der bekannteste Vertreter der Oligomycine.
Wirkung
Oligomycin A ist ein Inhibitor der ATP-Synthase. In Untersuchungen zur oxidativen Phosphorylierung wird es verwendet, um Atmung der Stufe 3, also ADP-induzierte Phosphorylierung,[3][4] zu inhibieren. Oligomycin A hemmt die ATP-Synthase durch Blockierung der Untereinheit Fo des Protonenkanals (o für Oligomycin[5][6]), der für die oxidative Phosphorylierung von ADP zu ATP benötigt wird (Energiegewinnung).
Die Hemmung der ATP-Synthese durch Oligomycin A reduziert den Elektronenfluss durch den Elektronentransportkanal auf signifikante Weise. Der Elektronenfluss kommt jedoch aufgrund von „Protonenlecks“, beziehungsweise mitochondrialer Entkopplung nicht ganz zum Erliegen. Diese Protonenlecks kommen durch erleichterte Diffusion mittels eines Uncoupling Proteins wie Thermogenin (auch bekannt als UCP1) zustande.[7]
Oligomycine
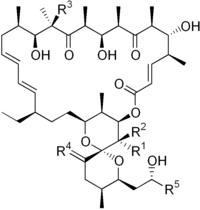
| |||||
|---|---|---|---|---|---|
| R1 | R2 | R3 | R4 | R5 | |
| Oligomycin A | CH3 | H | OH | H,H | CH3 |
| Oligomycin B | CH3 | H | OH | O | CH3 |
| Oligomycin C | CH3 | H | H | H,H | CH3 |
| Oligomycin D (Rutamycin A) |
H | H | OH | H,H | CH3 |
| Oligomycin E | CH3 | OH | OH | O | CH3 |
| Oligomycin F | CH3 | H | OH | H,H | CH2CH3 |
| Rutamycin B | H | H | H | H,H | CH3 |
| 44-Homooligomycin A | CH2CH3 | H | OH | H,H | CH3 |
| 44-Homooligomycin B | CH2CH3 | H | OH | O | CH3 |
Weblinks
- Spektrum.de, Lexikon der Biochemie: Oligomycin
- Spektrum.de, Lexikon der Biologie: Oligomycin
Literatur
- Liarisa A. Shchepina, Olga Y. Pletjushkina, Armine V. Avetisyan, Liora E. Bakeeva, Elena K. Fetisova, Denis S. Izyumov, Valeria B. Saprunova, Mikhail Y. Vyssokikh, Boris V. Chernyak, Vladimir P. Skulachev: Oligomycin, inhibitor of the F0 part of H+-ATP-synthase, suppresses the TNF-induced apoptosis. In: Oncogene. Band 21, Nr. 53, S. 8149–8157, November 2002, doi:10.1038/sj.onc.1206053 (freier Volltext).
Einzelnachweise
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Datenblatt Oligomycin A ≥95 % (HPLC) bei Sigma-Aldrich, abgerufen am 25. August 2017 (PDF).
- ↑ Oligomycine. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. August 2017.
- ↑ Experimenting with isolated mitochondria: state III respiration. David R. Caprette, Rice University, abgerufen am 25. August 2017 (english).
- ↑ B. Chance, G. R. Williams: Respiratory enzymes in oxidative phosphorylation. III. The steady state. In: The Journal of Biological Chemistry. 217, Nr. 1, 1955 S. 409–427, PMID 13271404 (freier Volltext).
- ↑ Y. Kagawa, E. Racker: Partial resolution of the enzymes catalyzing oxidative phosphorylation. 8. Properties of a factor conferring oligomycin sensitivity on mitochondrial adenosine triphosphatase. In: The Journal of Biological Chemistry. 241, Nr. 10, 1966 S. 2461–2466, PMID 4223640 (freier Volltext).
- ↑ Hans-Walter Heldt, Birgit Piechulla: Pflanzenbiochemie. Springer Spektrum, Berlin / Heidelberg 2015, ISBN 978-3-662-44398-9, S. 118, doi:10.1007/978-3-662-44398-9.
- ↑ M. Jastroch, A. S. Divakaruni, S. Mookerjee, J. R. Treberg, M. D. Brand: Mitochondrial proton and electron leaks. In: Essays in biochemistry. 47, Nr. 1, 2010, S. 53–67. doi:10.1042/bse0470053. PMID 20533900. Volltext bei PMC: 3122475.
- ↑ M. Nakata, T. Ishiyama, S. Akamatsu, Y. Hirose, H. Maruoka, R. Suzuki, K. Tatsuta: Synthetic studies on oligomycins. Synthesis of the oligomycin B spiroketal and polypropionate portions. In: Bulletin of the Chemical Society of Japan. 68, Nr. 3, 1995, S. 967–89. doi:10.1246/bcsj.68.967.
| Bitte den Hinweis zu Gesundheitsthemen beachten! |
| Dieser Artikel basiert ursprünglich auf dem Artikel Oligomycin A aus der freien Enzyklopädie Wikipedia und steht unter der Doppellizenz GNU-Lizenz für freie Dokumentation und Creative Commons CC-BY-SA 3.0 Unported. In der Wikipedia ist eine Liste der ursprünglichen Wikipedia-Autoren verfügbar. |