| Jewiki unterstützen. Jewiki, die größte Online-Enzyklopädie zum Judentum.
Helfen Sie Jewiki mit einer kleinen oder auch größeren Spende. Einmalig oder regelmäßig, damit die Zukunft von Jewiki gesichert bleibt ... Vielen Dank für Ihr Engagement! (→ Spendenkonten) |
How to read Jewiki in your desired language · Comment lire Jewiki dans votre langue préférée · Cómo leer Jewiki en su idioma preferido · בשפה הרצויה Jewiki כיצד לקרוא · Как читать Jewiki на предпочитаемом вами языке · كيف تقرأ Jewiki باللغة التي تريدها · Como ler o Jewiki na sua língua preferida |
Membranpotential
Ein Membranpotential ist die elektrische Spannung über eine elektrochemische Doppelschicht, die aus einer Membran und Raumladungen in angrenzenden Elektrolyten besteht. Handelt es sich bei der Membran um eine Biomembran wie die Zellmembran oder die Membran eines Zellorganells lautet die Vorzeichenkonvention „Innen- minus Außenpotential“.
In nebenstehendem Diagramm stehen die rote und die blaue Fläche für die positiven bzw. negativen Überschussladungen. Diese werden von der Membran daran gehindert, ihrer gegenseitigen Anziehung zu folgen. Die einhüllenden Kurven stellen die Ladungsdichte dar, die nach außen exponentiell abfällt. Das gilt auch für die elektrische Feldstärke (lila Kurve, i. W. das Wegintegral der Ladungsdichte), die abseits der Membran, falls dort kein Strom fließt, ganz verschwindet, sodass das elektrische Potential (grüne Kurve, Wegintegral der Feldstärke) dort jeweils konstant ist. Die Potentialdifferenz zwischen diesen konstanten Werten (grüner Pfeil) wird als Membranpotential bezeichnet, auch als Transmembranpotential oder gar elektrischer Gradient, worunter Physiker die Feldstärke verständen.
Ein Membranpotential kann wie bei einem Kondensator durch von außen zugeführte Ladung entstehen, etwa in den myelinisierten Abschnitten von Nervenfasern. Im biologischen Kontext bedeutender ist dagegen die Bildung des Membranpotentials durch Konzentrationsunterschiede auf beiden Seiten der Membran in Verbindung mit ionenselektiver Durchlässigkeit, gesteuerter Durchlässigkeit und aktivem Transport von Ionen durch die Membran.
Bei ausgedehnten Zellen, wie Nerven- oder Muskelzellen, variiert das Membranpotential räumlich. Es dient dort der Signalleitung bzw. -ausbreitung, in Sinneszellen und dem Zentralnervensystem auch der Informationsverarbeitung. In Chloroplasten und Mitochondrien dient das Membranpotential der energetischen Kopplung von Prozessen des Energiestoffwechsels: Ein Prozess, siehe Elektronentransportkette, transportiert Ionen gegen die Spannung und leistet dabei Arbeit, ein anderer, siehe ATP-Synthase, wird von der Potentialdifferenz angetrieben.
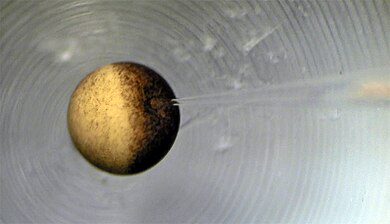
Die Messung von Membranpotentialen an mikroskopischen Strukturen, möglichst ohne elektrische, chemische und mechanische Beeinflussung, ist schwierig. Das Foto zeigt die Ableitung des Innenpotentials einer Zelle mit einer feinen Glaskapillare. An der Öffnung der Kapillare entsteht ein kleines Diffusionspotential, denn sie ist mit einem starken Elektrolyten in hoher Konzentration gefüllt, z. B. 3 M KCl, um einen definierten Übergang auf den metallischen Leiter zu gewährleisten, der sich in der Kapillare befindet und am Bildrand zu sehen ist. Die für die Messung des Membranpotentials notwendige Erfassung auch des Außenpotentials ist nicht mit im Bild.
Physiologische Werte
Die Phospholipid-Doppelschicht der Einheitsmembran hat einen hydrophoben Kern, der die Raumladungen gut fünf nm auseinanderhält. Das Ruhepotential tierischer Zellen liegt bei −70 mV. Daraus resultiert eine Feldstärke von über 107 V/m oder etwa das Vierfache der Durchschlagsfestigkeit von Luft. Bei Spannungen von 0,7 bis 1,1 Volt tritt Elektroporation ein.
Aus den Faktoren Feldstärke, Permittivitätszahl des Membranmaterials (≥ 2) und elektrische Feldkonstante ergibt sich eine Flächenladungsdichte von knapp 3·10−4 C/m², was sich mit der Faraday-Konstante in 3·10−6 mval/m² übersetzt.
Die für den exponentiellen Abfall der Raumladungsdichte charakteristische Debye-Länge beträgt unter physiologischen Bedingungen knapp einen Nanometer. In dieser Schicht befinden sich positive und negative bewegliche Ladungsträger in einer Flächenkonzentration von etwa 2·10−4 mval/m². Die Nettoladung macht also nur etwa 1 % der Ladungsdichte aus.
Potentialänderungen als Signale
Nervenzellen codieren Information in Gestalt von kurzfristigen Potentialänderungen. Diese lassen sich in zwei Gruppen unterteilen, die unterschiedliche Eigenschaften und Funktionen haben:
- graduierte Potentiale treten als Rezeptorpotential bei Sinneszellen auf und als postsynaptisches Potential bei chemischen Synapsen und der Motorischen Endplatte.
- Aktionspotentiale werden am Axonhügel und am Axon einer Nervenzelle oder an der subsynaptischen Membran von Muskelzellen erzeugt.
Vergleich in der Übersicht:
| graduiertes Potential | Aktionspotential | |
|---|---|---|
| 1 | amplitudenmoduliert | frequenzmoduliert |
| 2 | graduierte Amplitude | konstante Amplitude |
| 3 | nicht refraktär | refraktär |
| 4 | Summation möglich | keine Summation möglich („Alles-oder-Nichts-Prinzip“) |
| 5 | Ausbreitung passiv mit Amplitudenabfall | Ausbreitung aktiv mit Erhalt der Amplitude |
| 6 | keine Auslöseschwelle | definierte Auslöseschwelle |
| 7 | Depolarisation oder Hyperpolarisation mit anschließender Repolarisation | nur Depolarisation mit anschließender Repolarisation |
| 8 | unspezifische Kationenkanäle | schnelle, spannungsgesteuerte Natrium-Ionenkanäle |
| 9 | Dauer 40 bis 4000 ms | Dauer 4 ms |
Grundlagen
Ursache für die Diffusion der Ionen entlang eines Konzentrationsgefälles ist die Brownsche Molekularbewegung. Das Membranpotential kann diese Diffusion unterstützen, wenn Konzentrations- und Potentialgefälle in dieselbe Richtung wirken. Wenn das Potentialgefälle dem Konzentrationsgefälle entgegengerichtet ist, können die Ionen nur dann passiv entsprechend dem Konzentrationsgefälle diffundieren, wenn die Wirkung des Membranpotentials kleiner ist. Ist sie größer, dann diffundieren die Ionen gegen das Konzentrationsgefälle.
Diffusionspotential
- Modellversuch
Eine Kammer, die mit destilliertem Wasser gefüllt ist, wird durch eine omnipermeable Membran, zum Beispiel ein Filterpapier, in zwei Halbzellen unterteilt. In jeder Halbzelle befindet sich eine Elektrode, die beiden Elektroden sind durch ein Spannungsmessgerät miteinander verbunden. Wird in einer der beiden Halbzellen (zum Beispiel der rechten) Kochsalz (NaCl) aufgelöst, beobachtet man zunächst einen Anstieg der Spannung, die dann mit der Zeit allmählich wieder auf Null Volt sinkt.
- Erklärung:
Aufgrund des Konzentrationsgefälles diffundieren Natrium-Kationen und Chlorid-Anionen solange durch die Membran, bis in beiden Halbzellen die gleiche Konzentration an vorliegt. Das Natrium-Kation hat einen kleineren Durchmesser als das Chlorid-Anion, es kann leichter durch das Porensystem der Membran diffundieren. Deshalb steigt zu Beginn des Versuchs ihre Konzentration in der linken Halbzelle schneller als die der Anionen. Damit bildet sich ein Spannungsunterschied zwischen den beiden Halbzellen aus: links sind mehr positive, rechts mehr negative Ladungen.
Die Diffusionsgeschwindigkeit der Kationen wird aber gebremst. Einerseits wird das Konzentrationsgefälle schwächer, andererseits müssen die Kationen gegen das sich aufbauende Potentialgefälle diffundieren.
Dagegen wird die Diffusionsgeschwindigkeit der Anionen durch das Potentialgefälle erhöht.
Gleichgewichtspotential
- Modellversuch
Eine Kammer, die mit destilliertem Wasser gefüllt ist, wird durch eine selektive, semipermeable Membran, die nur das Kation passieren lässt, in zwei Halbzellen unterteilt. In jeder Halbzelle befindet sich eine Elektrode, die beiden Elektroden sind durch ein Spannungsmessgerät miteinander verbunden. Wird in einer der beiden Halbzellen (zum Beispiel der rechten) Kochsalz (NaCl) aufgelöst, beobachtet man zunächst einen Anstieg der Spannung, die dann als „Gleichgewichtsspannung“ erhalten bleibt.
- Erklärung
Aufgrund des Konzentrationsgefälles diffundieren die Natrium-Kationen durch die Membran. Aufgrund der Ladungstrennung baut sich ein Potentialgefälle auf: die Innenseite der Membran (linke Kammer) wird positiv, die Außenseite (rechte Kammer) negativ. Die Diffusionsgeschwindigkeit der Kationen wird aber gebremst. Einerseits wird ihr Konzentrationsgefälle schwächer, andererseits müssen die Kationen gegen das sich aufbauende Potentialgefälle diffundieren.
Das Diffusionsgleichgewicht ist dann erreicht, wenn die treibende Kraft des Konzentrationsgefälles für die Diffusion nach links genauso groß ist, wie die treibende Kraft des Potentialgefälles für die Diffusion nach rechts.
Im Gleichgewicht sind die Konzentrationen der Ionen innen von der Konzentration außen verschieden, deshalb ist eine Potentialdifferenz messbar.
Umkehrpotential
Das Umkehrpotential einer Membran mit geöffneten Kanälen ist das Membranpotential, bei dem der elektrische Nettostrom null ist. Das Umkehrpotential ist ein gewichteter Mittelwert der Gleichgewichtspotentiale der einzelnen permeablen Ionenarten, wobei die Gewichtung von deren Konzentration und Permeabilität abhängt, siehe unten Goldman-Hodgkin-Katz-Gleichung.
Mathematische Formalismen
Die Freie Enthalpie der Diffusion
An der Freien Enthalpie ΔG kann abgelesen werden, ob Teilchen bei einem gegebenen Konzentrations- und Potentialverhältnis durch eine Membran transportiert werden können:
- Ist ΔG = 0, liegt Gleichgewicht vor, die Menge der durch die Membran in eine Richtung diffundierenden Teilchen ist gleich der Menge der durch die Membran zurück diffundierenden Teilchen.
- Ist ΔG < 0 läuft der Transport in eine Richtung freiwillig ab, wobei Energie frei wird.
- Ist ΔG > 0 können die Teilchen nur unter Energieaufwand transportiert werden.
Die Freie Enthalpie kann auch als Maß des elektrochemischen Potentials angesehen werden, das sich aus den beiden Komponenten
- chemisches Potential (entspricht dem Konzentrationsgefälle) und
- elektrisches Potential (entspricht Potentialgefälle) zusammensetzt.
Chemisches Potential - Neutrale Teilchen
Für den Transport von außen nach innen (Import) gilt die Formel
Erläuterung:
- R: Allgemeine Gaskonstante R = 8,3143 J·mol−1·K−1
- T: Temperatur in Kelvin
- c(Ai), c(Aa): Stoffmengen-Konzentrationen des Stoffes A innen, außen
- ln: natürlicher Logarithmus
Für T = 298 K und Benutzung des dekadischen Logarithmus vereinfacht sich die Gleichung zu
- Wenn die Konzentration des Stoffes A innen genau so groß ist wie außen, ist ΔG = 0, es liegt Konzentrationsausgleich vor und es findet kein Stofftransport statt.
- Ist die Konzentration innen größer als außen, ist ΔG > 0, es findet kein passiver („freiwilliger“) Stofftransport von außen nach innen statt.
- Ist die Konzentration außen größer als innen, ist ΔG < 0, es findet Stofftransport von außen nach innen statt.
Elektrisches Potential - Geladene Teilchen
Anteil des Ladungstransportes an der Freien Enthalpie:
Erläuterung:
- Z: Die Ladungszahl Z entspricht der Ionenladung des zu transportierenden Teilchens. Sie ist für Kationen positiv, für Anionen negativ.
- F: Faraday-Konstante F = 96485 C·mol−1
- ΔΨ: Das Membranpotential ΔΨ lässt sich durch die Goldman-Gleichung (siehe unten) berechnen.
Elektrochemisches Potential
Für den Import geladener Teilchen gilt die Formel
Gleichgewichtspotential
Für den Gleichgewichtsfall (ΔG = 0) lässt sich das Gleichgewichtspotential ΔΨ0 für ein Ion nach folgender Formel berechnen:
für Z = 1 (bei Na+, K+) und T = 298 K ergibt sich bei Benutzung des dekadischen Logarithmus die vereinfachte Gleichung
Beispiel für ein Membranpotential (Mischpotential) von –53 mV bei 298 K:
| Ionensorte | ceq(Aaußen) | ceq(Ainnen) | ΔΨ0 | ΔG für einen Transport von außen nach innen |
|---|---|---|---|---|
| Na+ | 400 mmol/l | 20 mmol/l | +76 mV | +2,3 kJ/mol |
| K+ | 50 mmol/l | 440 mmol/l | −55 mV | −10,5 kJ/mol |
| Cl− | 108 | 560 | +43 mV | −11,0 kJ/mol |
Goldman-Hodgkin-Katz-Gleichung
Mittels der Goldman-Gleichung lässt sich das Membran-Gleichgewichtspotential ΔΨ berechnen:
Erläuterung:
- P: Permeabilität der Kanäle für Anionen (an) und Kationen (ka)
- c: Konzentration der Anionen und Kationen innerhalb (-i) oder außerhalb (-a) der Zelle
Siehe auch
- Ionenkanal, Transmembranprotein, Kaliumkanal, Transport (Biologie),
- Depolarisation (Physiologie), Hyperpolarisation (Biologie)
- Ruhemembranpotential, Aktionspotential
- Nernst-Planck-Gleichung
Literatur
- Jacob Kraicer, Samuel Jeffrey Dixon: Measurement and Manipulation of Intracellular Ions. Academic Press, 1995, ISBN 0-08-053646-8, Eingeschränkte Vorschau in der Google Buchsuche
Weblinks
| Dieser Artikel basiert ursprünglich auf dem Artikel Membranpotential aus der freien Enzyklopädie Wikipedia und steht unter der Doppellizenz GNU-Lizenz für freie Dokumentation und Creative Commons CC-BY-SA 3.0 Unported. In der Wikipedia ist eine Liste der ursprünglichen Wikipedia-Autoren verfügbar. |








![{\displaystyle \Delta \Psi ={\frac {RT}{F}}\cdot \ln {\frac {\Sigma [P_{\mathrm {ka} }\cdot c_{\mathrm {ka-a} }]+\Sigma [P_{\mathrm {an} }\cdot c_{\mathrm {an-i} }]}{\Sigma [P_{\mathrm {ka} }\cdot c_{\mathrm {ka-i} }]+\Sigma [P_{\mathrm {an} }\cdot c_{\mathrm {an-a} }]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/87dee5b9c7f394b13e4db4b03da54fc6496460cd)